In diesem Beitrag werden der grundsätzliche Anwendungsbereich der neuen Beschränkung (dazu unter A.), bestehende Ausnahmen und Übergangsfristen (dazu unter B. bis D.) sowie neu eingeführte Informationspflichten (dazu unter E. und F.) vorgestellt. Der vollständige Verordnungstext ist HIER abrufbar.
A. Anwendungsbereich (Spalte 1 und Spalte 2 Abs. 1)
Jenseits spezifischer Regelungen und Anforderungen folgt aus der Beschränkung ab dem Zeitpunkt ihres Inkrafttretens, dass synthetische Polymermikropartikel als solche oder, wenn die synthetischen Polymermikropartikel vorhanden sind, um eine gewünschte Eigenschaft zu verleihen, in Gemischen in einer Konzentration von ≥ 0,01 Gewichtsprozent nicht mehr in Verkehr gebracht werden dürfen (vgl. Abs. 1 des Eintrags Nr. 78 in Anhang XVII zu REACH).
Als synthetische Polymermikropartikel gelten dabei feste Polymere die beide der folgenden Bedingungen erfüllen:
- sie sind in Partikeln enthalten und machen mindestens 1 Gewichtsprozent dieser Partikel aus oder bilden eine kontinuierliche Oberflächenbeschichtung auf Partikeln;
- mindestens 1 Gewichtsprozent der unter Buchstabe a genannten Partikel erfüllt eine der folgenden Bedingungen:
- alle Dimensionen der Partikel sind gleich oder kleiner als 5 mm oder
- die Länge der Partikel ist gleich oder kleiner als 15 mm und das Verhältnis von Länge zu Durchmesser ist größer als 3.
Ausgenommen bleiben allerdings abbaubare oder wasserlösliche Polymere sowie natürliche Polymere, die nicht chemisch modifiziert wurden. Ebenso werden Polymere nicht vom Anwendungsbereich erfasst, die in ihrer chemischen Struktur keine Kohlenstoffatome enthalten.
Mit der Beschränkung wird allein das Inverkehrbringen von synthetischen Polymermikropartikeln als solchen oder in Gemischen verboten. Eine Regelung, die solche Partikel in, an oder auf Erzeugnissen in den Blick nimmt und das Inverkehrbringen jener Erzeugnisse verbieten würde, enthält die Verordnung indes nicht. Die Abgrenzung zwischen Stoffen/Gemischen einerseits und Erzeugnissen andererseits ist dabei nach den bekannten Kriterien entsprechend der ECHA-Leitlinie zu den Anforderungen für Stoffe in Erzeugnissen vorzunehmen. So werden z.B. Textilien oder Schuhe mit dekorativem Glitter regelmäßig ausschließlich als Erzeugnisse einzuordnen sein, sodass die Beschränkung auf derartige Produkte keine Anwendung findet.
B. Übergangsregelung für bereits in Verkehr gebrachte Ware (Spalte 2 Abs. 16)
Anders als bei vielen anderen Beschränkungen gem. REACH ist im Rahmen der Beschränkung von synthetischen Polymermikropartikeln kein genereller Aufschub für den Anwendungsbeginn vorgesehen. Die Beschränkung findet damit unmittelbar mit ihrem Inkrafttreten Anwendung. Dies bedeutet allerdings nicht, dass damit ebenso unmittelbar ein Verkaufsverbot einhergeht. Absatz 16 des Eintrags Nr. 78 in Anhang XVII zu REACH stellt – auch und gerade im Zusammenspiel mit dem Erwägungsgrund (60) zur Verordnung (EU) 2023/2055 – klar, dass vom Anwendungsbereich der Beschränkung erfasste Produkte (auch z.B. loser Glitter) weiter verkehrsfähig sind, soweit diese (erstmals) vor dem 17.10.2023 in Verkehr gebracht wurden. (vgl. hierzu mittlerweile ausdrücklich auch die Klarstellung des REACH-CLP-Biozid Helpdesks).
Damit kann grundsätzlich jedwede Ware auf allen Stufen der Lieferkette auch nach dem 17.10.2023 weiter vertrieben, d.h. weiter in Verkehr gebracht werden (vgl. Art. 3 Nr. 12 REACH), soweit diese bereits vor dem genannten Termin auf vorgelagerten Stufen der Lieferkette im Geltungsbereich der REACH-Verordnung in Verkehr gebracht war. Ausreichend, aber auch erforderlich ist daher, dass die Ware vor dem 17.10.2023 von einem Akteur in der Lieferkette an einen anderen abgegeben wurde oder vor dem 17.10.2023 in den Geltungsbereich der REACH-Verordnung eingeführt wurde. Unter diesen Voraussetzungen sind daher auch Lagerbestände weiterhin verkehrsfähig.
Selbstverständlich sollten betroffene Unternehmen jedoch hinreichend genau dokumentieren können, dass und welche Produkte konkret bereits vor dem 17.10.2023 in Verkehr gebrachten waren und deshalb ihre Verkehrsfähigkeit auch nach diesem Stichtag nicht verlieren (z.B. über Chargennummern, Lieferscheine, Inventurdaten zum Stichtag o.ä.).
C. Anwendungs- und produktspezifische Ausnahmen
Die Beschränkung enthält darüber hinaus einige generelle Ausnahmen, etwa für Verwendungen in Industrieanlagen (mit weitergehenden Informationspflichten ab dem 17.10.2025 und zusätzlichen Berichtspflichten), Arzneimitteln, EU-Düngeprodukten, Lebensmittelzusatzstoffen, In-vitro-Diagnostika oder auch Lebens- und Futtermitteln (Spalte 2 Abs. 4).
Zudem finde die Beschränkung keine Anwendung, soweit die Partikel durch technische Mittel so eingeschlossen sind, dass eine Freisetzung in die Umwelt verhindert wird, wenn sie während der vorgesehenen Endanwendung vorschriftsmäßig verwendet werden, wie z.B. bei Ionenaustauscherharzen, Windeln oder Binden. Ferne bleiben solche synthetischen Polymermikropartikel von der Beschränkung ausgenommen, deren physikalische Eigenschaften während der vorgesehenen Endanwendung dauerhaft so verändert werden, dass das Polymer nicht mehr in den Anwendungsbereich dieses Eintrags fällt. Auch synthetische Polymermikropartikel, die während der vorgesehenen Endverwendung dauerhaft in eine feste Matrix integriert werden, bleiben ausgenommen. Erfasst werden hier v.a. Partikel in Gemischen, die im Rahmen der Endanwendung aushärten oder sich sonst verfestigen (Spalte 2 Abs. 5).
Da in diesen Fällen aber gleichwohl Freisetzungen von synthetischen Polymermikropartikeln nicht vollständig ausgeschlossen werden können, sind gerade auch für einige diese Produkte ab dem 17.10.2025 bzw. ab dem 17.10.2026 Anweisungen für die Verwendung und Entsorgung für gewerbliche Anwender und die breite Öffentlichkeit zur Verfügung zu stellen, in denen erläutert wird, wie die Freisetzung synthetischer Polymermikropartikel in die Umwelt verhindert werden kann (Spalte 2 Abs. 7 und 8).
Die Art und Weise der Erfüllung dieser zusätzlichen Informationspflicht ist in der Beschränkung nur recht allgemein umschrieben. Erforderlich ist jedenfalls eine Angabe in Form von deutlich sichtbarem, lesbarem und unauslöschlichem Text bzw. in Form von Piktogrammen. Die Angaben können auf einem Etikett, der Verpackung oder in der Packungsbeilage gemacht werden. Ist ein Sicherheitsdatenblatt nach Art. 31 REACH erforderlich, sind die Informationen dort aufzunehmen. Ergänzende (aber nicht ausschließliche) Verwendungen digitaler Zugangsformen bleibt ebenfalls möglich. Die entsprechenden Instruktionen sind, soweit keine Piktogramme verwendet werden, in den Amtssprachen der Mitgliedstaaten abzufassen, in denen der Stoff oder das Gemisch in Verkehr gebracht werden. Die Mitgliedstaaten können hierzu aber auch abweichende Regelungen treffen, zum Beispiel hinsichtlich der Akzeptanz auch anderer Sprachfassungen oder des Erfordernisses mehrsprachiger Hinweise (Spalte 2 Abs. 10).
Nicht erforderlich ist in diesem Zusammenhang jedoch, dass auch ein expliziter Hinweis darauf gegeben wird, dass das jeweilige Produkt Mikroplastik enthält. Diese Anforderung besteht allein für bestimmte kosmetische Mittel (Spalte 2 Abs. 9).
D. Produkt-/verwendungsspezifische Übergangsfristen
Gerade kosmetische Mittel werden, zusammen mit anderen Produkten, von einer Vielzahl von – mitunter langen – Übergangsfristen erfasst, so dass die Beschränkung erst zu einem späteren Zeitpunkten Anwendung findet und entsprechende Produkte mit synthetischen Polymermikropartikeln erst nach Ablauf der so geschaffenen Übergangsfristen der Beschränkung unterfallen. Diese Übergangsfristen sind in Spalte 2 Abs. 6 wie folgt enthalten:
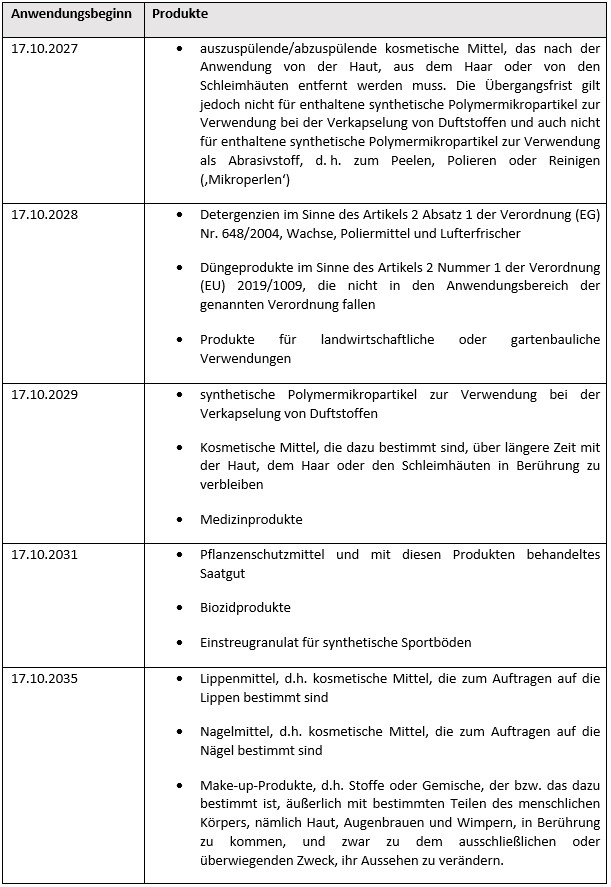
Die verlängerten Übergangsfristen gelten jeweils nur soweit die in Rede stehenden Produkte nicht anderen, früher endenden Übergangsfristen zugeordnet werden können. Produkte, die insofern verschiedenen Übergangsfristen zugeordnet werden könnten, werden grundsätzlich zum jeweils früheren Termin der Beschränkung unterfallen.
E. Informationspflichten gegenüber der ECHA (Spalte 2 Abs. 12)
Ab dem Jahr 2027 müssen Lieferanten von Arzneimitteln und Tierarzneimitteln, Lebensmittelzusatzstoffen und In-vitro-Diagnostika, sowie von Produkten die synthetische Polymermikropartikel enthalten aber von der Beschränkung ausgenommen sind, weil diese durch technische Mittel eingeschlossen sind oder deren physikalische Eigenschaften während der vorgesehenen Endanwendung dauerhaft verändert werden oder diese in eine feste Matrix integriert werden, weitergehende Informationspflichten gegenüber der Europäischen Chemikalienagentur (ECHA) erfüllen.
Neben der Beschreibung der Endverwendungen, für die die synthetischen Polymermikropartikel im jeweils vorangegangenen Kalenderjahr in Verkehr gebracht wurden, sind auch für jede Endverwendung allgemeine Informationen über die Identität der im vorangegangenen Kalenderjahr in Verkehr gebrachten Polymere zu übermitteln. Ergänzt wird dies um eine Verpflichtung zur Abgabe einer Schätzung der Menge synthetischer Polymermikropartikel, die im vorangegangenen Kalenderjahr in die Umwelt freigesetzt wurden, einschließlich der Menge synthetischer Polymermikropartikel, die während des Transports in die Umwelt freigesetzt wurden.
Die entsprechenden Informationen werden den Mitgliedstaaten von der ECHA zur Verfügung gestellt.
F. Informationsverpflichtung gegenüber Vollzugsbehörden (Spalte 2 Abs. 14 und 15)
Nicht unterschätzt werden sollte letztlich auch die Verpflichtung von Herstellern, Importeuren und nachgeschalteten industriellen Anwendern von Produkten, die synthetische Polymermikropartikel enthalten, den zuständigen Behörden auf deren Ersuchen spezifische Informationen über die Identität und die Funktion der von der Beschränkung erfassten Polymere an die Hand zu geben. Dies wird insbesondere deshalb nicht trivial werden, da die spezifischen Informationen über die Identität der Polymere ausreichen müssen, um die Polymere eindeutig zu identifizieren. Dabei verweist die Beschränkung auf Anforderungen zur Bestimmung der Stoffidentität nach Anhang VI REACH, obwohl die dort enthaltenen Vorgaben für Zwecke der Registrierung von Stoffen eingeführt wurden und Polymere als solche gerade nicht der Registrierungspflicht unterliegen (vgl. Art. 6 Abs. 3 REACH). Dessen ungeachtet sind folgende Angaben auf Ersuchen der Behörden zur Verfügung zu stellen:
- Name und andere Bezeichnungen des Stoffes
- Name(n) laut IUPAC-Nomenklatur; falls nicht vorhanden, andere internationale chemische Bezeichnung(en)
- Andere Namen (allgemeine Bezeichnung, Handelsname, Abkürzung)
- EG-Nummer, d. h. die Einecs-, ELINCS- oder NLP-Nummer oder die von der Agentur zugeteilte Nummer (sofern vorhanden und sachdienlich)
- CAS-Bezeichnung und CAS-Nummer (sofern vorhanden)
- Sonstiger Identifizierungscode, z. B. Zollnummer (sofern vorhanden)
- Angaben zu Summen- und Strukturformel oder Kristallstruktur des Stoffes
- Summen- und Strukturformel (einschließlich Smiles-Notation und anderer Repräsentation, sofern vorhanden) und Beschreibung der Kristallstruktur(en)
- Angaben zur optischen Aktivität und zum typischen Anteil von (Stereo-)Isomeren (falls zutreffend und sachdienlich)
- Molekulargewicht oder Molekulargewichtsbereich
- Alle für die Identifizierung des Stoffes erforderlichen qualitativen analytischen Daten wie z. B. Ultraviolett-, Infrarot-, NMR-, Massenspektrografie- oder Diffraktionsdaten
- Alle für die Identifizierung des Stoffes erforderlichen quantitativen Analysedaten, z. B. Daten aus der chromatographischen, titrimetrischen oder Elementaranalyse oder Diffraktionsdaten
- Beschreibung der Analysemethoden oder Angabe der bibliografischen Daten, die für die Identifizierung des Stoffes erforderlich sind (einschließlich Identifizierung und Quantifizierung seiner Bestandteile und gegebenenfalls der Verunreinigungen und Zusatzstoffe). Die Beschreibung besteht aus den zugrunde liegenden Versuchsprotokollen und der entsprechenden Auswertung der unter den Nummern 2.3.1 bis 2.3.6 genannten Ergebnisse. Die Angaben müssen die Reproduktion der Methoden ermöglichen.
Die Verpflichtung gilt unmittelbar und ohne weitergehende Übergangsfirst. Es ist allerdings zu beachten, dass die Verpflichtung nicht für nachgeschaltete gewerbliche Anwender gilt. Auch reine Händler sind nicht betroffen, da diese nach Art. 3 Nr. 13 REACH gerade nicht vom Begriff des „nachgeschalteten Anwenders“ erfasst werden. Spezifische Informationsersuchen im Rahmen von allgemeinen Marktüberwachungsmaßnahmen im Einzel- oder Onlinehandel dürften daher nicht zu erwarten sein.
Zudem reduziert sich die Relevanz der entsprechenden Auskunftspflicht selbst auf Ebene der nachgeschalteten Anwender. Liegen die Informationen dort nicht vor, so haben diese die Information lediglich innerhalb von sieben Tagen nach Eingang des Ersuchens bei ihrem Lieferanten anzufordern und die Behörde unverzüglich darüber zu unterrichten. Die Verpflichtung des Lieferanten erschöpft sich in diesem Fall in der Anfrage beim Lieferanten. Letzter hat sodann die angeforderten Informationen innerhalb von 30 Tagen direkt an die zuständige Behörde, die die Informationen angefordert hat, zu übermitteln oder aber an den nachgeschalteten industriellen Anwender weiterzugeben, der diese sodann unverzüglich an die zuständigen Behörden weiterzuleiten hat. Umgekehrt hat die Behörde, soweit sie die Informationen direkt erhält, den nachgeschalteten industriellen Anwender zu informieren.
G. Fazit und Ausblick
Die Beschränkung von synthetischen Polymermikropartikeln zeichnet sich aufgrund der Regelungssystematik – generelles Verbot mit spezifischen, mehrschichtigen Ausnahme- und Übergangsregelungen – durch eine hohe Komplexität aus. Es steht zu erwarten, dass diese Vorgehensweise in Zukunft bei einer Vielzahl weiterer Beschränkungen gewählt wird, wie z.B. der Vorschlag zur Beschränkung von PFAS anschaulich unterstreicht.
Für zahlreiche Produkte mit synthetischen Polymermikropartikeln bietet die Beschränkung Ausnahmen oder längere Übergangsregelungen. Trotz des grundsätzlich unmittelbaren Anwendungsbeginns werden daher Produkte mit „Mikroplastik“ nicht unmittelbar aus dem Markt entfernt. Es steht aber zu erwarten, dass der konkrete Handlungsdruck auch und gerade im Zusammenhang mit ergänzenden Informations- und Berichtspflichten selbst weiterhin gestattete Verwendungen zunehmend unattraktiv machen wird und in zahlreichen Branchen und Lieferketten die Verfügbarkeit entsprechender Produkte auch schon vor dem Auslaufen von Übergangszeiträumen eingeschränkt sein wird.
Haben Sie zu dieser News Fragen oder wollen Sie mit dem Autor über die News diskutieren? Kontaktieren Sie gerne: Martin Ahlhaus