A. REACH
Für die Anwendung und Fortentwicklung der Verordnung (EG) Nr. 1907/2006 (REACH) wird 2022 ein besonders wichtiges Jahr. Neben einer Vielzahl von Anpassungen und Ergänzungen des bestehenden Rechtsrahmens, steht das laufende Jahr ganz im Zeichen der bevorstehenden Novellierung der Verordnung.
I. Termine
Die REACH-Verordnung selbst sieht aktuell bereits einige konkrete Termine vor, die im laufenden Jahr zu beachten sein werden.
1. Prüfung von Versuchsvorschlägen
So ist nach Art. 43 Abs. 2 lit. c) REACH vorgesehen, dass bis zum 01.06.2022 für alle Registrierungen betreffend Phase-in-Stoffe mit Versuchsvorschlägen, die bis zum 01.06.2018 eingegangen sind, von der Europäischen Chemikalienagentur (ECHA) entsprechende Entscheidungsentwürfe nach Art. 40 Abs. 3 REACH erstellt werden. Damit dürfte eine Reihe von Registranten im laufenden Jahr mit entsprechenden Verfahren zu rechnen haben.
2. Zulassungskandidatenliste
Bereits zum 17.01.2022 hat die ECHA vier weitere Einträge in die Kandidatenliste für das Zulassungsverfahren unter REACH aufgenommen:
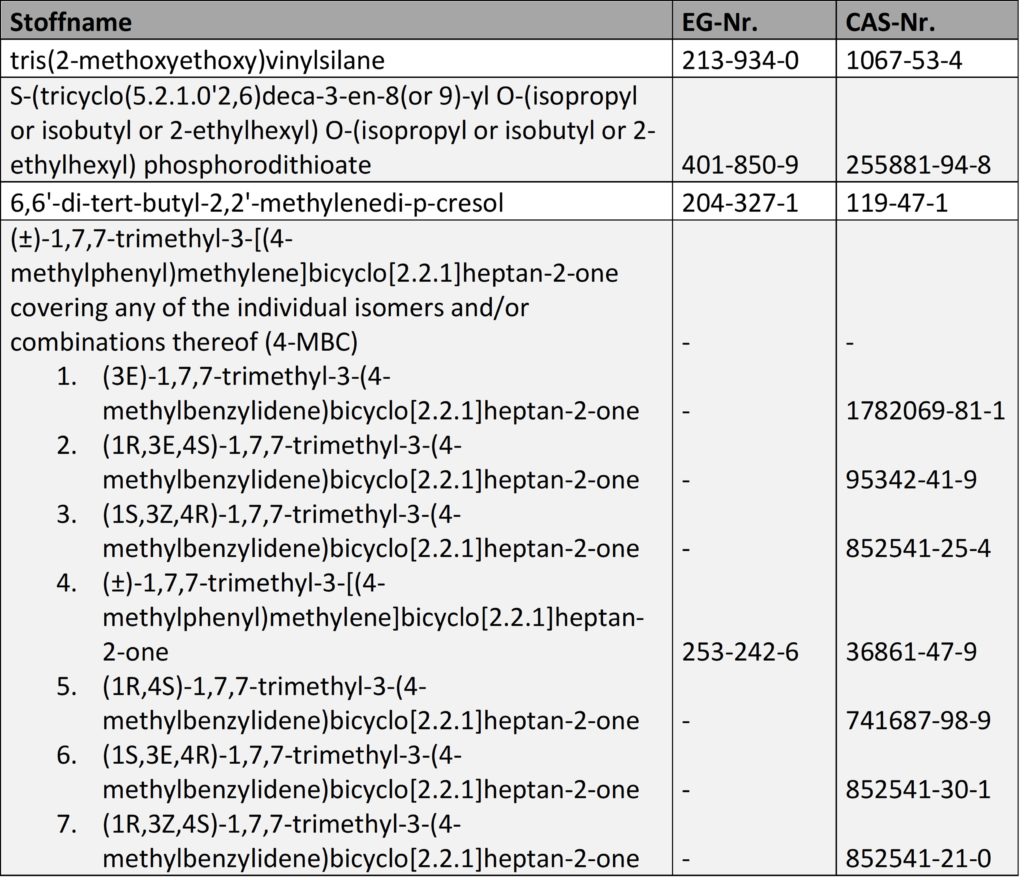
Die Liste umfasst nun 223 Einträge, die unmittelbar sowohl für die Kommunikation in der Lieferkette nach Art. 33 REACH wie auch für Meldungen in die SCIP-Datenbank zu beachten sind. Für etwaige Notifizierungspflichten nach Art. 7 Abs. 2 REACH gilt für die per 17.01.2022 neu aufgenommenen Stoffe zunächst noch eine Übergangsfrist von weiteren sechs Monaten (vgl. Art. 7 Abs. 7 REACH).
Zudem wurde der Eintrags von PFDA geändert. Der bisherige Gruppeneintrag “Nonadecafluorodecanoic acid (PFDA) and its sodium and ammonium salts” umfasste vormals mit “Decanoic acid, nonadecafluoro-, sodium salt” und “sodium nonadecafluorodecanoate” zwei Einträge. Da diese beiden Einträge jedoch den gleichen Stoff bezeichnen, wurde der Eintrag “Decanoic acid, nonadecafluoro-, sodium salt” gestrichen.
Entsprechend der üblichen Praxis der ECHA steht zur Mitte des Jahres eine weitere Ergänzung der Kandidatenliste zu erwarten.
3. Zulassungsanträge
Für insgesamt fünf zulassungspflichtige Stoffe gemäß Anhang XIV zu REACH endet im laufenden Jahr die Frist für die Einreichung von Zulassungsanträgen. Betroffen sind:
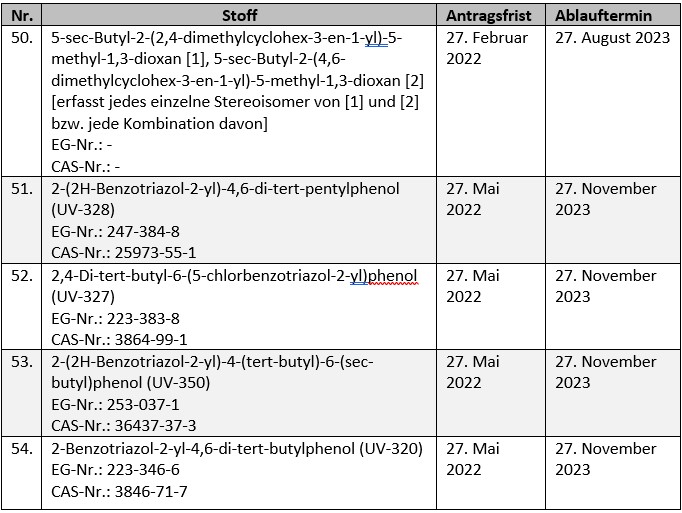
Ohne fristgerechten Antrag dürfen die in Rede stehenden Stoffe nur noch bis zu den jeweiligen Ablaufterminen verwendet werden. Dies gilt auch, wenn ein Zulassungsantrag nach Ablauf der Antragsfrist eingereicht wird. In diesem Fall bleibt zunächst die Zulassungsentscheidung abzuwarten, bis die entsprechende Verwendung wieder aufgenommen werden darf.
4. Beschränkungen
Auch für zwei der jüngeren Beschränkungen stehen in 2022 maßgebliche Anwendungstermine an. So darf Diisocyanate nach Eintrag Nr. 74 in Anhang XVII zu REACH bereits ab dem 24.02.2022 weder als Stoff noch als Bestandteil in anderen Stoffen oder Gemischen für die industrielle oder gewerbliche Verwendung in Verkehr gebracht werden, es sei denn, die Konzentration von Diisocyanaten einzeln und in Kombination beträgt weniger als 0,1 Gew.-% oder der Lieferant stellt weitergehende Informationen zur sicheren Verwendung zur Verfügung und gibt auf dem Etikett an, dass ab dem 24.08.2023 vor der industriellen oder gewerblichen Verwendung eine angemessene Schulung erfolgen muss.
Bereits seit dem 04.01.2022 gelten zudem Verwendungsverbote für bestimmte Stoffe in Tätowierfarben. Einzelheiten hierzu sind unserem Blog-Beitrag vom 05.01.2022 zu entnehmen
II. Weitere Änderung der Informationsanforderungen
Bereits mit Verordnung (EU) 2021/979 wurde ein erstes Paket zur Änderung der Informationsanforderungen für Registrierungen in den Anhängen VII bis XI der REACH-Verordnung umgesetzt. Die Verordnung ist bereits seit dem 08.07.2021 in Kraft gilt seit dem 08.01.2022. Die wesentliche Zielsetzung der damit verbundenen, punktuellen Nachjustierung einzelner Datenanforderungen lag vor allem in der Klarstellung und Präzisierung der Vorgaben.
Zwischenzeitlich hat der REACH-Regelungsausschuss im schriftlichen Verfahren einstimmig auch dem zweiten Paket zur Änderung der Informationsanforderungen in den REACH-Anhängen VI bis X zugestimmt. Neben sprachlichen Klarstellungen sollen vor allem die Datenanforderungen in Bezug auf CMR-Eigenschaften präzisiert werden. Der entsprechende Verordnungsentwurf liegt dem Rat und dem Europäischen Parlament zur Prüfung bis zum 19.02.2022 vor. Danach kann die Kommission den Entwurf im Amtsblatt der EU veröffentlichen. Nach Inkrafttreten ist auch hier eine Übergangsfrist von sechs Monaten vorgesehen. Wie schon die vorangegangene Verordnung wird auch diese Änderung der Anhänge der REACH-Verordnung nicht nur bei der erstmaligen Erstellung und Einreichung von Registrierungsdossiers zu berücksichtigen sein. Vielmehr werden die Änderungen auch bei Aktualisierungen bestehender Registrierungen zu beachten sein.
III. Weitere Risikomanagementmaßnahmen
Auch im laufenden Jahr wird ein zentraler Aspekt der Umsetzung der REACH-Verordnung auf der Fortführung der integrierten regulatorischen Strategie der ECHA liegen. Die von der ECHA veröffentlichte Liste über die Bewertung des regulatorischen Bedarfs enthält derzeit 714 Einträge (Stand: 13.01.2022). Es steht auch für 2022 zu erwarten, dass die ECHA betroffene Registranten von Stoffen, für die neue Risikomanagementmaßnahmen erwartet werden, kontaktieren wird. Regelmäßig werden die Registranten aufgefordert, ihre Registrierungsdossiers zu aktualisieren und die Verwendungsinformationen zu überprüfen. Zudem sollen die Registranten in die Lage versetzt werden, die etwaigen Auswirkungen der vorgeschlagenen Maßnahmen vorherzusehen.
Aktuell läuft etwa noch ein Konsultationsverfahren unter Federführung der deutschen Bundesanstalt für Arbeitsschutz und Arbeitsmedizin (BAuA) zur Erstellung einer RMO-Analyse zu Fasermaterialien (Stoffe/Gemische/Erzeugnisse), die Partikel mit einer Länge größer 5 μm, einem Durchmesser kleiner 3 μm und einem Länge-zu-Durchmesser-Verhältnis, welches größer als 3:1 (WHO-Faserkriterium) ist, enthalten und biobeständig sind
IV. Fortlaufende Konsultationsverfahren
Entsprechend der Vielzahl potentieller regulatorischer Ansätze sollten Unternehmen und Verbände auch im Jahr 2022 mit großer Sorgfalt und Aufmerksamkeit die verschiedenen Konsultationsverfahren verfolgen. Dies gilt in besonderer Weise für Aufforderungen zur Einreichung von Bemerkungen und zur Vorlage von Nachweisen, künftige Beschränkungen und Zulassungspflichten wie auch etwaige Versuchsvorschläge. Nur mit zielgerichteter Mitwirkung in den entsprechenden Konsultationsverfahren von Seiten der Industrie lassen sich regulatorische Fehlentwicklungen vermeiden.
V. Revision der REACH-Verordnung
Die sicherlich weitreichendsten Veränderungen werden aber mit der Revision der REACH-Verordnung verbunden sein. Ziel ist dabei weiterhin, dass bis Ende 2022 ein Kommissionsentwurf zur Umsetzung der Anpassungen vorliegt. Dabei wird es im Laufe des Jahres eine Vielzahl von Möglichkeiten und Notwendigkeiten für die Mitwirkung von Industrievertretern geben.
Die wesentliche Zielsetzungen einer Anpassung der REACH-Verordnung folgen dabei der „Chemicals Strategy for Sustainability”. Folglich werden Maßnahmen zur zielgerichteten Umsetzung von Anforderungen für sogenannte „safe and sustainable by design chemicals“, zur Einführung von „non-toxic material cycles“ und der Etablierung eines „essential use concepts” im Fokus stehen. Daneben werden die gefährlichsten Stoffe wie auch endokrine Disruptoren ebenso in den Blick genommen, wie Bewertungskriterien für Gemische.
Als Querschnittsthema wird der Ansatz „one substance, one assessment“ für eine Reihe produktrechtlicher Anforderungen besondere Beachtung erlangen. Hierzu ist für 2022 ein horizontaler Vorschlag für die Neuverteilung von Aufgaben im Bereich der betroffenen EU-Agenturen, EFSA, ECHA, EMA und EEA, vorgesehen. Nicht übersehen werden sollte zudem, dass die Chemikalienstrategie auch eine „Null-Toleranz“-Politik bei Verstößen gegen bestehende Anforderungen vorsieht. Zu diesem Zweck sollen Vollzugsmaßnahmen gestärkt werden, sowohl an den Außengrenzen der EU als auch auf Ebene der einzelnen Mitgliedstaaten
B. CLP
Im Rahmen der Verordnung (EG) Nr. 1272/2008 (CLP) liegt der Fokus neben der laufenden Fortschreibung harmonisierter Einstufungs- und Kennzeichnungsvorgaben vor allem auf der Anpassung und Änderung der Verordnung selbst.
Ein erstes zentrales Projekt stellt in diesem Zusammenhang die öffentliche Konsultation zur Initiative der Europäischen Kommission zur Vereinfachung und Digitalisierung der Kennzeichnungsvorschriften für Chemikalien dar. Die Konsultation läuft noch bis zum 16.02.2022.
Darüber hinaus wird die angedachte Revision der CLP-Verordnung vor allem auf die Einführung neuer Gefahrenklassen (EDs, PBTs, etc.), die Verbesserung der Einstufung (harmonisierte Einstufung wie auch Selbsteinstufung), die Anpassung von Kennzeichnungsbestimmungen (Faltetiketten, Ausnahmen bei kleinen Verpackungen usw.), die Anforderungen an den Online-Verkauf und eine etwaige Anpassung des Anwendungsbereichs der CLP-Verordnung gerichtet sein. Aufgrund der weitreichenden Auswirkungen sollten Unternehmen die entsprechenden Entwicklungen sorgfältig verfolgen
C. Biozide
Für das laufende Jahr steht die Fortführung von Verfahren betreffend die Genehmigung von Wirkstoffen im Vordergrund, um die Zielsetzungen des Arbeitsprogramms zu erreichen. Daneben werden selbstverständlich laufende Verfahren betreffend die Zulassung von Biozidprodukten auf nationaler wie europäischer Ebene fortzuführen sein.
I. Produktzulassungen
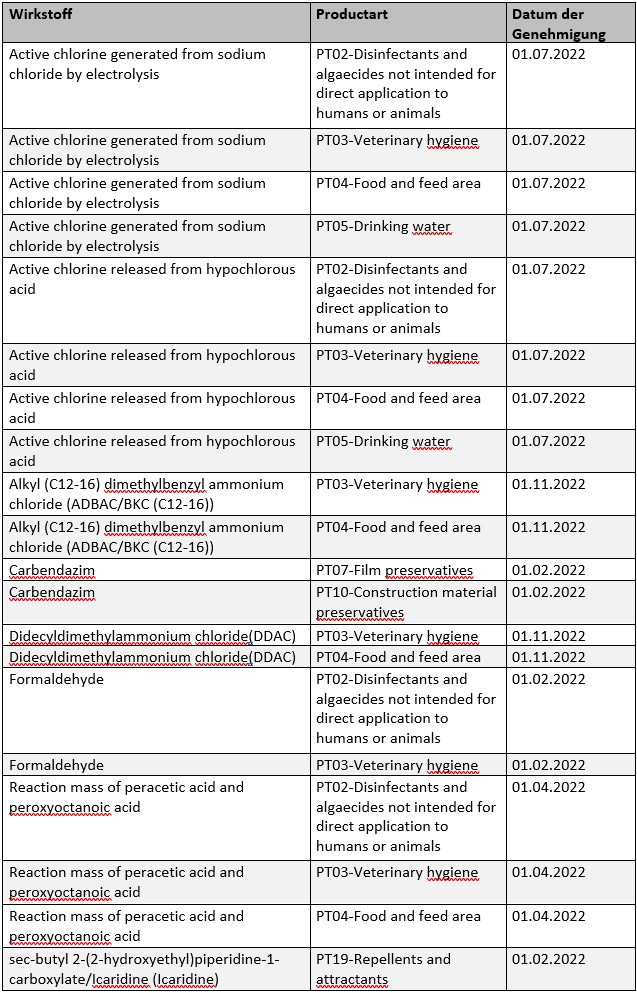
Im Anwendungsbereich der Verordnung (EU) Nr. 528/2012 (BPR) beginnt auch im Jahr 2022 für eine Reihe von Wirkstoffen die Genehmigungsdauer. Bis zum jeweiligen Datum der Genehmigung sind von betroffenen Unternehmen entsprechende Zulassungsanträge für Biozidprodukte zu stellen, um in den Genuss weitergehender Übergangsfristen zu kommen (vgl. Artikel 89 BPR).
II. Meldung von Biozidprodukten
Ab dem 01.01.2022 gilt für Biozidprodukte ein neues Meldeverfahren. Die bisherige ChemBiozidMeldeV wurde zu diesem Zweck durch die neue Biozidrechts-Durchführungsverordnung (ChemBiozidDV, BGBl. I 2021, Nr. 57) abgelöst. Auf dieser Grundlage sind künftig nicht nur Biozidprodukte mit Altwirkstoffen meldepflichtig, die aufgrund einer anwendbaren Übergangsregelungen weiterhin auch ohne Zulassung in Deutschland verkehrsfähig sind. Auch auf dem Markt bereitgestellte Biozidprodukte sind künftig von der Meldepflicht erfasst. Nach Angaben der BAuA wird ein entsprechend überarbeitetes, neues Online-Portal ab dem 26.01.2022 zur Verfügung stehen.
Die Meldungen für Biozidprodukte, die unter die Übergangsregelungen für Altwirkstoffe fallen, werden dabei aus dem bisherigen Melderegister übernommen. Die durch die ChemBiozidDV neu eingeführten Informationspflichten sind für solche Alt-Meldungen aus der Zeit vor dem 26.08.2021 bis zum 31.03.2022 zu erfüllen. Die neuen Informationspflichten erstrecken sich dabei vor allem auf
- die Angabe der Wirkstoffkonzentration in dem Biozidprodukt
- Angaben zur Antragsstellung gemäß § 28 Abs. 8 Satz 2 ChemG
- Angaben zu Art. 95 Biozid-Verordnung
- Bestätigung der dem Biozidprodukt zugeschriebenen Wirkung.
D. Fazit und Ausblick
Insgesamt werden Unternehmen somit auch im Jahr 2022 vor erhebliche Herausforderungen bei der Umsetzung der regulatorischen Anforderungen im Bereich des Chemikalienrechts gestellt. Im laufenden Jahr wird für betroffene Unternehmen und Verbände eine besondere Herausforderung auch und gerade darin bestehen, die vielfältigen Konsultationsprozesse und Änderungsbestrebungen im Rahmen der Chemikalienstrategie für Nachhaltigkeit im Blick zu behalten.
Haben Sie zu dieser News Fragen oder wollen Sie mit dem Autor über die News diskutieren? Kontaktieren Sie gerne: Martin Ahlhaus